A. Numération sanguine normale NFS
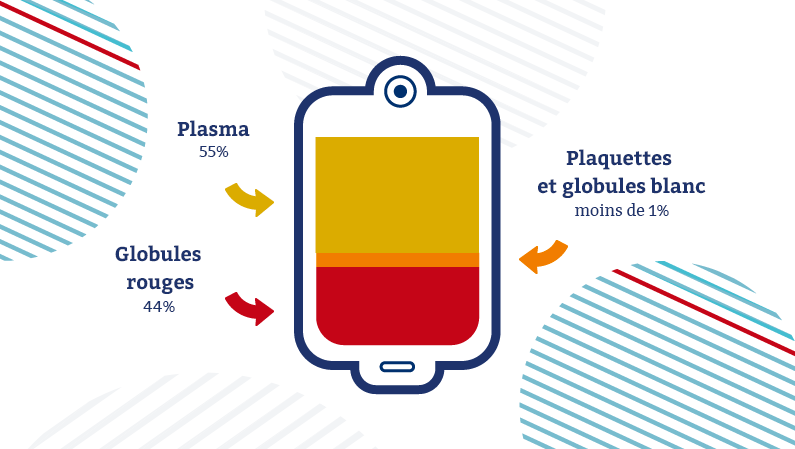
Le sang est un liquide de notre corps qui coule dans les vaisseaux sanguins. Il est formé d’un liquide jaune clair : le sérum ou plasma dans lequel circulent les différentes cellules : les globules rouges, les globules blancs et les plaquettes.
• Erythrocytes, hématies ou globules rouges. Ils transportent l’oxygène des poumons aux tissus grâce à l’hémoglobine (qui donne la couleur rouge au sang). Numération entre 4.5 et 6.5 millions (le globule rouge vit 120 jours, il naît dans la moelle osseuse et il meurt dans la rate). Si moins, anémie, fatigue, vertiges.
• Leucocytes ou globules blancs. Ils ont un rôle immunitaire contre les infections. Numération entre 4000 et10000. Si moins, plus grande sensibilité aux infections bactériennes (neutropénie).
On y distingue * les polynucléaires neutrophiles
éosinophiles
basophiles
*les lymphocytes sont les globules blancs les plus évolués, ils sont les chefs de la réponse immunitaire contre les agressions : agents infectieux, dangereux microbes ou cellules cancéreuses ou étrangères.
* les monocytes
• Les plaquettes. Elles sont indispensables à une bonne coagulation du sang. Numération entre 150000 et 500000. Si trop (thrombocytose), risque de thrombose (caillot qui bouche le vaisseau) ; si pas assez (thrombopénie), risque de saignements (purpura, ecchymoses, épistaxis ou hémorragies digestives).
B. D’où viennent ces différents composants
La moelle osseuse est un tissu situé dans la cavité centrale de tous nos os mais surtout dans les os plats. (bassin, sternum, côtes, etc.) Elle fabrique de façon continue des cellules appelées cellules souches. Les cellules qui sont dans cette moelle « mûrissent » pour donner les cellules matures du sang : les globules rouges, les globules blancs et les plaquettes. Ces cellules ne sont libérées dans le sang que lorsqu’elles sont parvenues à maturité. Il est anormal de trouver dans le sang des cellules de la moelle osseuse.
Ne pas confondre moelle osseuse et moelle épinière (structure nerveuse se trouvant dans notre colonne vertébrale).
C. Les leucémies :
Il y a 1800 nouveaux cas de leucémie par an en France. En France environ 600 enfants par an sont touchés par la leucémie.
Invasion de la moelle osseuse par des cellules anormales de la lignée blanche, dérivées des cellules productrices des éléments du sang. Dans les leucémies aiguës, la différenciation des cellules de la moelle osseuse est bloquée à un stade de cellules immatures déformées, appelées « blastes ». Ces blastes s’accumulent et envahissent la moelle osseuse ainsi que le sang. Ils perturbent la production de globules rouges, de globules blancs normaux et de plaquettes.
Dans les leucémies chroniques, il y a uniquement prolifération des cellules jeunes qui coexistent avec des globules blancs matures.
1) Les circonstances de la découverte : fatigue persistante, teint pâle, signes de saignement (hématomes, pétéchies ou purpura à cause du manque de plaquettes), fièvre, ganglions. La recherche de ganglions se fait par palpation du cou, des creux axillaires et de l’aine par le médecin traitant. Il existe aussi des ganglions profonds dans le thorax ou dans l’abdomen que l’on explore en faisant un scanner TAP (thoraco- abdomino-pelvien).
Attention, ces manifestations ne sont pas spécifiques de la leucémie.
2) Diagnostic
• L’examen de la formule sanguine au microscope montre des blastes dans le sang et des taux anormaux des différentes variétés de globules et des plaquettes (augmentation du nombre de globules blancs et diminution importante du nombre de globules rouges et des plaquettes).
Attention : un excès de globules blancs ne correspond pas forcément à une leucémie. En effet, les infections, par exemple, provoquent une augmentation des globules blancs normaux. Dans ce cas les cellules ne sont pas malignes. Certains aspects à la NFS sont trompeurs et nécessitent un contrôle.
Le myélogramme (examen microscopique de la moelle osseuse obtenue par ponction sternale ou dans l’os iliaque) confirme la présence des cellules leucémiques et permet de préciser le type de leucémie.
On peut prélever la moelle osseuse de deux façons, par ponction sternale ou par biopsie médullaire (encore appelée biopsie osseuse).
o La ponction sternale
Après anesthésie locale de la peau, la ponction sternale est effectuée sur la partie bombée du sternum, avec une aiguille appelée trocart. La moelle osseuse, qui a la consistance d’un sang un peu épais, est aspirée par une seringue et le prélèvement est ensuite étalé sur des lames et examiné au microscope pour un examen cytologique ou myélogramme.
o La biopsie ostéomédullaire
Elle complète la ponction sternale si les renseignements fournis par cette dernière sont insuffisants (par exemple si la moelle contient peu de cellules ou si elle est très fibreuse).
Elle est effectuée, sous anesthésie locale, sur un os du bassin, au dessus de la fesse. Le prélèvement osseux est effectué à l’aide d’un trocart. Après préparation et coloration, le tissu osseux est examiné au microscope pour un examen histologique.
3) Les différentes leucémies. Elles se distinguent par la lignée sanguine de globules blancs à l’origine de la prolifération (polynucléaires ou lymphocytes ou monocytes) et par le pourcentage de cellules leucémiques présentes dans la moelle osseuse. Les leucémies sont dites lymphoïdes lorsque ce sont des lymphocytes qui sont concernés. On les appelle myéloïdes si ce sont les polynucléaires qui sont touchés.
Les principales :
Si les blastes représentent + de 50% des cellules de la moelle osseuse
• Leucémies aiguës myéloblastiques (LAM)
• Leucémies aiguës lymphoblastiques (LAL)
• Leucémies chroniques myéloblastiques ou lymphoblastiques
Ce n’est pas une classification officielle puisqu’il existe des subdivisions multiples et variées pour chacune d’entre elles.
4) Les causes
Les LAM peuvent survenir à tout âge.
Les LAL atteignent plutôt les enfants, maladie maligne la plus courante chez les enfants (30% des cancers pédiatriques)
Les leucémies chroniques touchent l’adulte presque exclusivement.
Les causes des leucémies ne sont pas évidentes. Cependant on relève des facteurs qui peuvent parfois les déclencher (exposition à des radiations ionisantes, benzène, arsenic, trisomie 21). Elles ne sont ni héréditaires, ni contagieuses.
5) Les traitements
Le choix des traitements se fait à partir d’une RCP (Réunion de Concertation Pluridisciplinaire entre professionnels de santé).
Dans les leucémies aiguës
Dès le diagnostic et le traitement établis, le malade est hospitalisé dans le service d’onco-hématologie et un cathéter central est posé.
C’est une perfusion que l’on met dans une grosse veine profonde en général au niveau du cou, L’extrémité du tuyau est glissée sous la peau pour sortir quelques centimètres plus bas sur la paroi du thorax Ce geste est réalisé au bloc opératoire sous anesthésie locale et implique des conditions d’asepsie importantes. Il permet d’infiltrer la chimio sans risques et d’effectuer les bilans sanguins quotidiens ainsi que le passage de produits sanguins ou alimentaires quand c’est nécessaire.
➢ Chimiothérapie
Un protocole est une combinaison de plusieurs agents de chimiothérapie nécessaire au traitement.
a) traitement d’induction : corticoïdes (pour les LAL) + chimiothérapie
* a pour but d’atteindre la rémission complète qui sera confirmée par un myélogramme.
*dure 4 à 6 semaines avec une période d’aplasie transitoire (diminution de toutes les cellules sanguines) pendant laquelle le malade reste en chambre protégée car sans défense : les globules blancs et notamment les polynucléaires neutrophiles (moins de 500/mm3) n’étant plus là pour le protéger contre les agents infectieux. La chimiothérapie ayant détruit les mauvaises comme les bonnes cellules, il est indispensable de transfuser du sang et des plaquettes et en cas de fièvre de mettre en place une couverture antibiotique.
La sortie d’aplasie est le moment où la moelle fabrique à nouveau des polynucléaires neutrophiles que l’on retrouve dans le sang.
Dans certains cas des facteurs de croissance sont prescrits pour accélérer la sortie d’aplasie.
• Dans le cas d’une LAL, on y associe une ponction lombaire (PL) pour dépister la présence de cellules leucémiques dans le liquide céphalo-rachidien, et une chimiothérapie intrathécale (injection de chimio par ponction lombaire) pour protéger les méninges (il s’agit, sous anesthésie locale, d’enfoncer une aiguille, la plus fine possible à un niveau sous-jacent à l’extrémité terminale de la moelle épinière, entre deux vertèbres lombaires, le plus souvent entre la quatrième et la cinquième).
*On refait un nouveau myélogramme pour savoir si le malade est en rémission complète avec un retour à la normale du sang et de la moelle osseuse.
L’étude du myélogramme montre ou pas la disparition de toutes les cellules malades. Si elles ont toutes été éliminées on parle alors de rémission.
On ne peut pas parler de guérison. On sait à ce moment-là que la maladie ne se voit plus mais qu’elle pourrait être encore là, invisible dans quelques cellules résiduelles qui ont échappé à la chimio.
On sait aussi d’après les études, qu’à ce stade, si on arrête le traitement définitivement, la maladie reviendra.
b) Traitements de consolidation et intensification. Ils consistent en plusieurs cycles de chimio (pour consolider la rémission complète et éliminer une éventuelle maladie résiduelle). Une ponction lombaire peut y être associée dans le cas d’une LAL.
De façon générale, la chimiothérapie entraîne certains effets secondaires : nausées, vomissements, diarrhée, constipation, mucites buccales, alopécie (perte des cheveux), fatigue.
c) Traitement d’entretien sur une durée de 2 à 3 ans et surveillance prolongée.
Le suivi sera réalisé par des prises de sang et des myélogrammes à intervalles réguliers, afin de détecter précocement d’éventuelles rechutes.
➢ Greffe de moelle : en cas d’échec de la chimio ou de reprise évolutive de la maladie, jusqu’à 70ans pour certains cas et le malade étant en rémission complète.
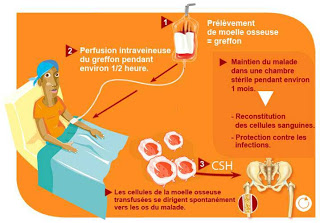
On remplace la moelle malade par une moelle saine. Le malade sera placé en chambre stérile.
On distingue :
a) L’allogreffe où l’on prélève des cellules souches saines sur un donneur autre que le patient. Elle dépend d’un donneur totalement compatible. (tests sanguins de compatibilité, groupage H.L.A, d’abord dans la fratrie).
La probabilité de trouver deux individus compatibles en dehors de la fratrie est de 1 chance sur 1 million. C’est pourquoi chaque nouvelle inscription sur le fichier des donneurs compte et apporte une chance supplémentaire de guérison pour les malades (voir chapitre « Don de soi »).
b) L’autogreffe où l’on prélève des cellules souches saines par cytaphérèse sur le patient lui-même. Elle est peu utilisée pour les leucémies parce que par définition, la maladie est la cellule souche.
c) La greffe haplo identique, plus récente, pour laquelle le donneur n’est qu’à moitié compatible (père, mère, frère, sœur, demi-frère, demi-sœur).
d) La greffe de sang de cordon.
L’allogreffe se fait après une chimio très intense et une radiothérapie de tout le corps pour détruire toutes les cellules (les cellules leucémiques comme les normales) de la moelle osseuse.
Puis, on met une perfusion d’un liquide qui ressemble à du sang, ce sont les cellules souches de la moelle osseuse du donneur. Les cellules qui s’y trouvent vont tout de suite trouver leur place dans les os et reprendre peu à peu leur travail.
Si la greffe de moelle est la plus facile à réaliser, elle est un traitement lourd sur le plan immunologique. La nouvelle moelle osseuse peut rejeter l’organisme du receveur. C’est le contraire d’une greffe d’organe. On appelle cela « la réaction du greffon contre l’hôte » (GVH).
Les lymphocytes attaquent principalement la peau, les intestins et le foie ; on retrouve une peau rouge, des manifestations digestives avec une diarrhée, une jaunisse et parfois de la fièvre. Ces signes nécessitent parfois la ré-hospitalisation du malade. Un médicament appelé la cyclosporine est administré pendant 6 mois à un an après la greffe pour éviter ce genre de réaction.
Ces risques peuvent parfois s’avérer mortels et l’éventualité d’une rechute n’est jamais à exclure.
Chaque étape de la maladie est difficile et parfois à la souffrance physique s’ajoutent des troubles psychologiques.
On parle de guérison complète lorsqu’une rémission dure 10 ans.
Dans les leucémies chroniques
Les leucémies chroniques sont traitées différemment selon qu’il s’agit d’une leucémie myéloïde chronique (LMC) ou d’une leucémie lymphoïde chronique (LLC) :
• Le traitement de la leucémie lymphoïde chronique (qui dépend du stade de la maladie) est essentiellement basé sur la chimiothérapie. Il arrive toutefois que des leucémies de ce type, dont le diagnostic est très précoce et qui n’évoluent pas, soient simplement mises sous « surveillance active ».
• Les traitements de la leucémie myéloïde chronique (due à la présence d’une anomalie chromosomique nommée « chromosome de Philadelphie ») permettent désormais à plus de 90% des patients de mener une vie quotidienne sans problème majeur. Depuis le début des années 2000, la leucémie myéloïde chronique bénéficie d’une thérapie ciblée, le Glivec, qui a radicalement changé la prise en charge et le pronostic de ce cancer. Aujourd’hui, le Glivec a été remplacé, d’autres médicaments ont contribué globalement à faire baisser le prix du traitement de la leucémie myéloïde chronique.
6) Quelques chiffres sur la leucémie chez les enfants:
➢ En France, 29 % des 1 700 nouveaux cas de cancers diagnostiqués chez l’enfant de moins de 15 ans sont des leucémies. Ce sont les cancers les plus fréquents chez les enfants.
➢ Chez l’enfant, 80 % des leucémies aiguës sont dites lymphoïdes ou lymphoblastiques (LAL). Parmi ces cas, 80 % sont des LAL de la lignée B (touchant le développement des lymphocytes B), dites communes.
➢ Dans plus de 90 % des cas, les causes d’une leucémie aiguë lymphoblastique (LAL) restent inconnues. Pour les 10 % restants, les facteurs de risque reconnus sont d’ordre génétique ou toxique.
➢ En 1947, la leucémie aiguë restait la dernière grande maladie mortelle de l’enfance. Elle tuait en quelques mois tous les enfants qu’elle frappait.
➢ En France, près de 470 cas de leucémie sont diagnostiqués chez les enfants chaque année.
➢ Aujourd’hui, le taux de survie à 5 ans (délai après lequel une rechute est exceptionnelle) est de près de 82 % pour les enfants atteints de leucémie aiguë lymphoblastique et d’environ 60 % pour les leucémies aiguës myéloblastiques qui touchent principalement des enfants de moins de 1 an.
➢ Chez les adolescents âgés entre 15 et 20 ans, environ 150 à 200 nouveaux cas sont diagnostiqués chaque année. Les adolescents et les jeunes adultes sont plus à risque de rechuter que les enfants.
Ainsi peut-on mesurer les progrès accomplis par près de 70 années de combat contre la leucémie.
